Ароматические соединения (арены) - очень
интересная группа органических веществ. Они
привлекают внимание исследователей необычным
строением и свойствами, многоплановыми
превращениями, широкими возможностями
практического применения.
Арены заметно выделяются из всех других
классов органических веществ свой высокой
стабильностью и понятие "ароматичность",
объединяющее циклические плоские  -электронные системы, -
одно из ключевых в органической химии,
характеризует не только геометрию, но и
электронное строение, пути и механизмы
превращений.
-электронные системы, -
одно из ключевых в органической химии,
характеризует не только геометрию, но и
электронное строение, пути и механизмы
превращений.
Плоские циклические высокосимметричные
структуры бензола, нафталина и других подобных
соединений на первый взгляд исключают
возможность появления стереоизомерии в этом
ряду. Однако спиральные молекулы различных
гелиценов, не содержащие ни одного
тетраэдрического атома углерода, могут быть
разделены на энантиомеры (как, например,
гексагелицены 1 и 2,
отличающиеся необыкновенно высокой оптической
активностью).
Одна из ярких особенностей поведения
аренов в различных реакциях состоит в том, что
они способны претерпевать скелетные
изомеризации. Установлено, что валентные изомеры
бензола и других аренов [например, бензол Дьюара
(3), бензол Ладенбурга (4), бензол Хюккеля (5)], легко
получаемые из различных предшественников, в том
числе и из аренов, участвуют во многих
термических и фотохимических превращениях
последних. Меньшая термодинамическая
стабильность валентных изомеров 3 - 5 по сравнению
с бензолом часто предопределяет их переход в
бензол.
Ароматические соединения - это не только
классические арены и гетарены. К ним относятся
также качественно новые в структурном отношении
вещества - фуллерены, впервые описанные в 1985 г.
Один из представителей этой группы трехмерных
соединений - фуллерен С60.
После выделения бензола в
индивидуальном состоянии (М.Фарадей, 1825 г.) до
того момента, когда для него была предложена
структурная формула (А.Кекуле, 1865 г.), прошло
значительное время. В эти годы были сделаны очень
важные открытия, касающиеся поведения в
различных реакциях как бензола, так и многих
других аренов. Можно отметить реакции, найденные Н.Зининым
(превращение нитробензола в анилин,
J.prakt.Chem. 1842, Bd. 27, S. 140), Г.Кольбе
(синтез салициловой кислоты из фенола по
Кольбе-Шмитту, Ann. 1860, Bd. 113, S. 125),
которые, наряду со многими другими, составляют
основу технологического получения различных
функциональных производных аренов и в настоящее
время.
РАЗДЕЛ "А"
Номенклатура ароматических соединений.
Ароматичность карбо- и гетероциклов.
Общие закономерности реакций электрофильного
замещения аренов
(нитрование, галогенирование, сульфирование)
1.Напишите структурные формулы
следующих соединений:
п-бромотолуол,
о-хлороанилин,
2,4-динитрохлорбензол,
м-диэтинилбензол,
о-ди-третбутилбензол,
2,4,6-трибромоанизол,
п-хлорофенол,
м-нитротолуол,
о-бромохлоробензол,
п-хлоростирол,
кумол,
4-(N,N-диметиламино)бензальдегид,
2,4,6-трибромобензойная кислота,
3,5-дихлоротолуол,
2,4,6-тринитротолуол,
2-фенилпентан,
1,3,5-трифенилбензол,
1,1,2-трифенилциклопропан,
4,4'-динитробифенил,
хлористый бензил,
a,a'-дибромодибензилкетон,
бензиловый спирт,
1,3-дифенилпропан,
9,10-дибромоантрацен,
1-хлоро-3-метил-1-фенилбутан,
2-фенил-2-пропанол,
п-ксилол,
м-крезол,
2,4,6,-трибромфенол,
1,5-диаминонафталин,
4-метил-1-нафтол,
8-метил-1-нафтол
2.Назовите следующие соединения:
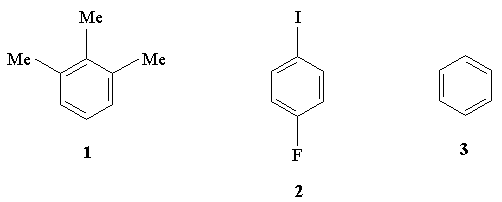
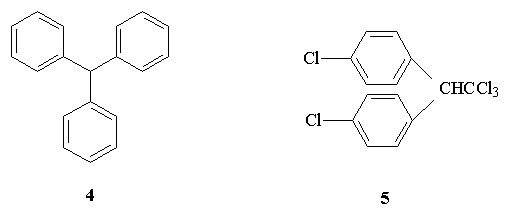
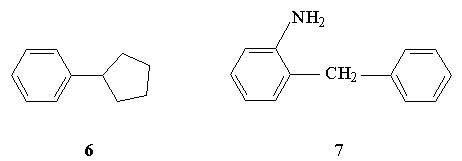
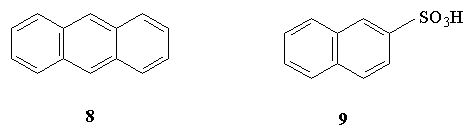
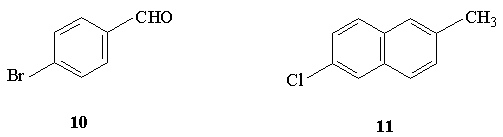
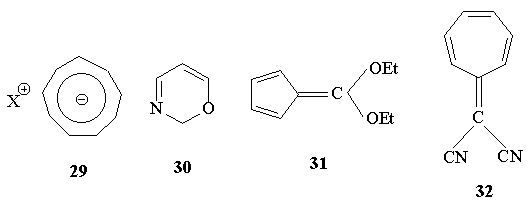
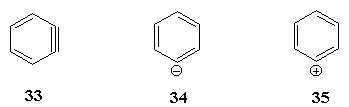
3.Какие из приведенных ниже соединений
можно отнести к ароматическим, неароматическим,
антиароматическим?
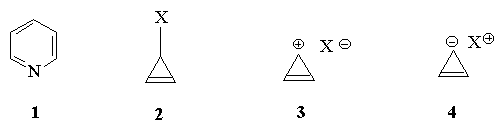
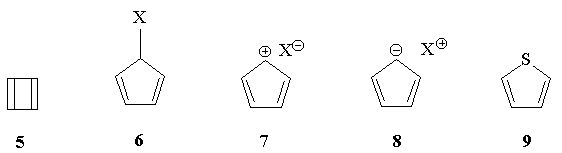
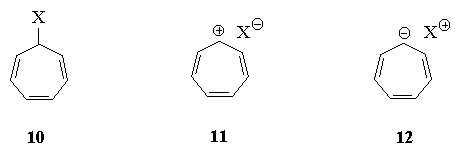
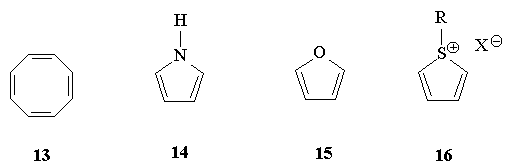
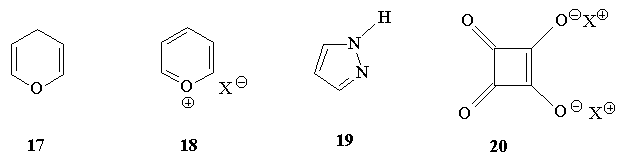
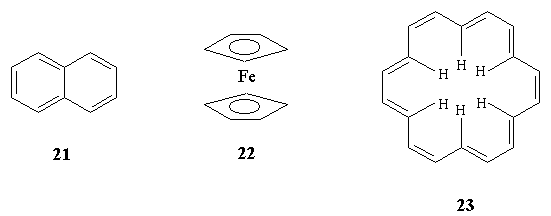
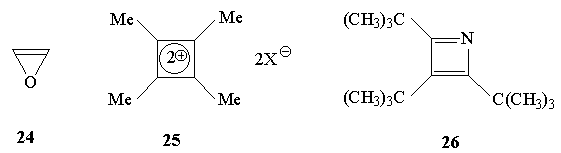
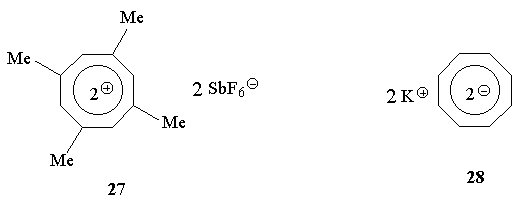
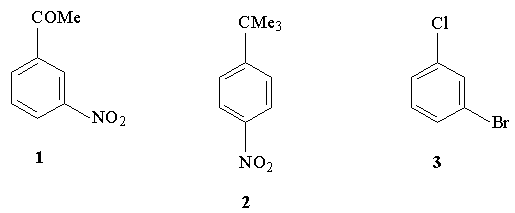
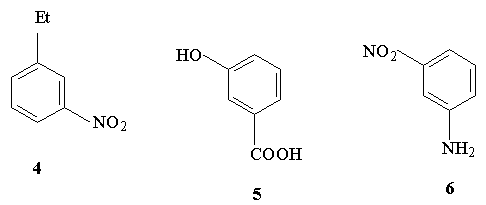
4.Среди предложенных ниже соединений
укажите примеры согласованного и
несогласованного влияния групп, контролирующих
вступление третьего заместителя в бензольное
кольцо в условиях реакций электрофильного
замещения.
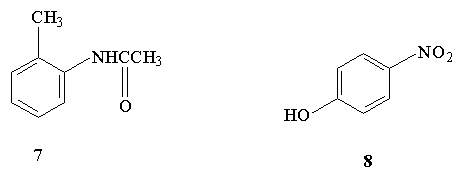
5.Сравнение дипольных моментов
бензофенона и дифенилциклопропенона указывает
на бульшую полярность циклического кетона по
сравнению с арил-, диарил- и циклоалкилкетонами.
Предложите объяснение высокой полярности
производного циклопропенона.

6.Основность N,N-диметиланилина в 2 раза
выше, чем основность анилина. В то же время при
переходе от 2,4,6-тринитроанилина к
N,N-диметил-2,4,6-тринитроанилину основность
последнего возрастает в 40000 раз. Почему введение
двух метильных групп в амино-группу
2,4,6-тринитроанилина так резко увеличивает
основность полинитропроизводного анилина?
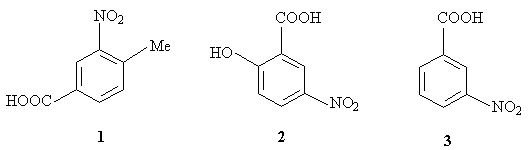
7.Предложите структуры соединений,
которые могут быть использованы для синтеза
следующих производных бензола и нафталина с
помощью реакций электрофильного замещения.
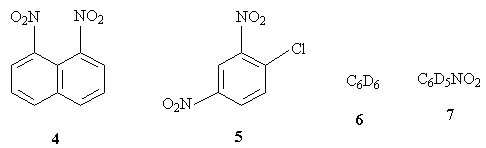
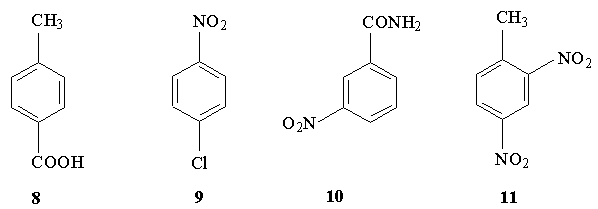
8. Напишите структуры продуктов
нитрования следующих производных бензола и
укажите условия, в которых указанная Вами
ориентация реализуется:
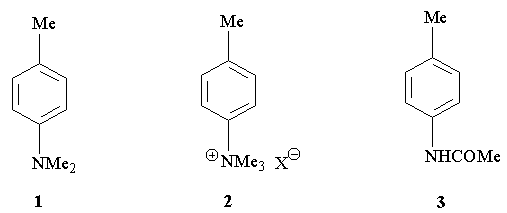
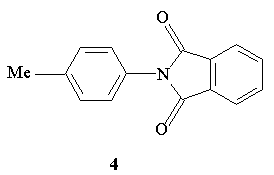
9.Известно, что нитрование толуола
приводит к смеси о-, м- и п-нитротолуолов,
в которой о- и п-изомеры в сумме
составляют до 95%. В отличие от толуола  ,
, ,
, -трифторотолуол
в сходных условиях предпочтительно образует
3-нитро-
-трифторотолуол
в сходных условиях предпочтительно образует
3-нитро- ,
, ,
, -трифторотолуол. Предложите
объяснение наблюдаемой ориентации в реакции
нитрования трифтортолуола.
-трифторотолуол. Предложите
объяснение наблюдаемой ориентации в реакции
нитрования трифтортолуола.
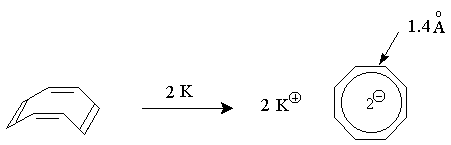
10.Легко протекающая реакция
циклооктатетраена (ЦОТ) в эфирном растворе с
щелочными металлами завершается образованием
солей циклооктатетраенил-дианионов, имеющих
плоское строение. Выскажите Ваши соображения по
поводу:
а) высокой активности ЦОТ в таких превращениях,
б) изменения геометрии восьмичленного цикла при
переходе от нейтральной молекулы ЦОТ к соли
дианиона.
11. Каждый из трех изомеров (1, 2 и
3) дибромбензола поместили в отдельные
колбочки. На основании нижеприведенных фактов
определите их строение.
а) нитрование соединения 1 (т. пл. 87 °С)
приводит только к одному нитродибромбензолу,
б) соединения 2 и 3 являются жидкостями,
в) нитрование соединения 2 дает 2 изомерных
нитродибромбензола,
г) при нитровании соединения 3 получено 3
нитродибромбензола.
12. Среди нижеприведенных заместителей
в ароматическом ядре укажите
12.1. орто, пара-ориентанты,
12.2. мета-ориентанты,
12.3. активирующие заместители в реакциях
электрофильного замещения, дезактивирующие
заместители в реакциях электрофильного
замещения.
-NH3+, -NMe2, CH3C(O)-, -SO3H,
-C? N, -NO2, -NMe3+, -C(O)H, Alk-, -NHC(O)CH3,
-OH, -OCH3, -OC(O)CH3, -NH2, -Cl, -Br, -I, -C(O)NH2,
-C(O)OCH3, CH3CH=CH-, CF3-, C6H5-,
-CH2NO2.
Объясните Ваши отнесения.
13. Обработка N,N-диметиланилина
нитрующей смесью (HNO3 + H2SO4, 5-10 °C)
и далее водным аммиаком привела с выходом около
60% к м-нитро-N,N-диметиланилину. Приведите
схему превращения и объясните причину
наблюдаемого места вступления нитрогруппы в
ароматическое ядро.
14. На основании рассмотрения всех
возможных резонансных структур ароматического
соединения фенантрена объясните, почему связь
С(9)-С(10) более подобна двойной С=С связи, чем
другие углерод-углеродные связи в молекуле.
15. Какие продукты Вы ожидаете в
приведенных ниже превращениях:
15.1. фенетол + Br2 (Fe) 
15.2. бензальдегид + Br2 (Fe) 
15.3. ацетанилид + (HNO3 + HSO4) 
15.4. кумол + (HNO3 + HSO4) 
15.5. этилбензоат + (HNO3 + HSO4) 
15.6. дейтеробензол + (H2O + H2SO4)

16. Приведите резонансные структуры для
карбокатионного интермедиата, предполагаемого в
реакции электрофильного замещения нафталина при
С(1); рассмотрите только структуры, сохранившие
ароматичность в незамещенном кольце. Объясните,
почему замещение при С(1) предпочтительнее
замещения при С(2).(ответ)
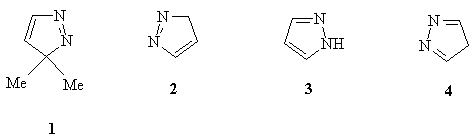
17. Среди приведенных ниже пиразолов 1-4 укажите
ароматические и неароматические соединения.
Мотивируйте сделанные Вами отнесения.
18. К раствору 4-нитроанилина (0.32 мол) в 400 мл
уксусной кислоты добавляют при перемешивании и
температуре бани 65оС раствор брома (0.64 мол)
в 240 мл уксусной кислоты. После перемешивания при
этой же температуре в течение 1 часа реакционную
смесь охлаждают и выливают в смесь 1 л воды с 500 г
льда. После промывания полученного осадка водой,
высушивания при 100оС и перекристаллизации
из монометилового эфира этиленгликоля получают
с выходом 96% вещество в виде зеленовато-желтых
призм с т. пл. 201-202оС, в ИК спектре которого
найдены полосы поглощения при 3490, 3380, 1600, 1510 см-1
. Напишите уравнение реакции, назовите
полученное соединение, сделайте отнесение
приведенных полос поглощения.
(ответ)
19.
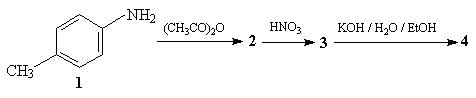
Назовите исходное соединение 1. Приведите
структуры, а также назовите соединения 2-4,
образующиеся в ходе вышеприведенных
превращений.
Для установления структур соединений
используйте данные ИК спектров и спектров ПМР,
приведенные в Таблице.
Таблица
21. Исходя из толуола с использованием
подходящих реагентов, не прибегая к реакциям
алкилирования и ацилирования ароматического
ядра, получите:
21.1. 4-(п-толил)бутанол-1,
21.2. п-толуиловый альдегид.
21.3. 4-дейтеротолуол (ответ)
22. Установите строение ароматического
углеводорода С9Н12, при обработке
которого бромом в присутствии бромного железа
образуется единственное бромпроизводное. (ответ)
23. Предложите реагенты и условия осуществления
приведенных ниже превращений:24. Какое исходное лучше использовать для
одностадийного синтеза 3-бромо-5-нитробензойной
кислоты: 3-бромобензойную кислоту или
3-нитробензойную кислоту? Объясните. (ответ )
25. Приведите условия нижеприведенных
превращений.